Consideraciones prácticas#
Le recomendamos consultar Microtutor y MyScope para obtener explicaciones interactivas de muchos de estos conceptos.
Selección de objetivos#
Los objetivos del microscopio tienen una serie de características que deben tenerse en cuenta al decidir qué objetivo es el adecuado para su experimento.
Magnification and resolution: the higher the numerical aperture (NA) of the lens, the finer the resolution one can obtain in one’s sample. The NA is calculated as \(NA=RI * sin(θ)\), relating both to the refractive index of the sample, glass, and immersion media as well as the range of angles of emitted light that can be collected into the lens. Unless special techniques are used, the typical limit of resolution is calculated as \(d = λ / 2NA\), meaning the resolution is set both by the NA of the lens but also by the wavelength of light used for imaging.
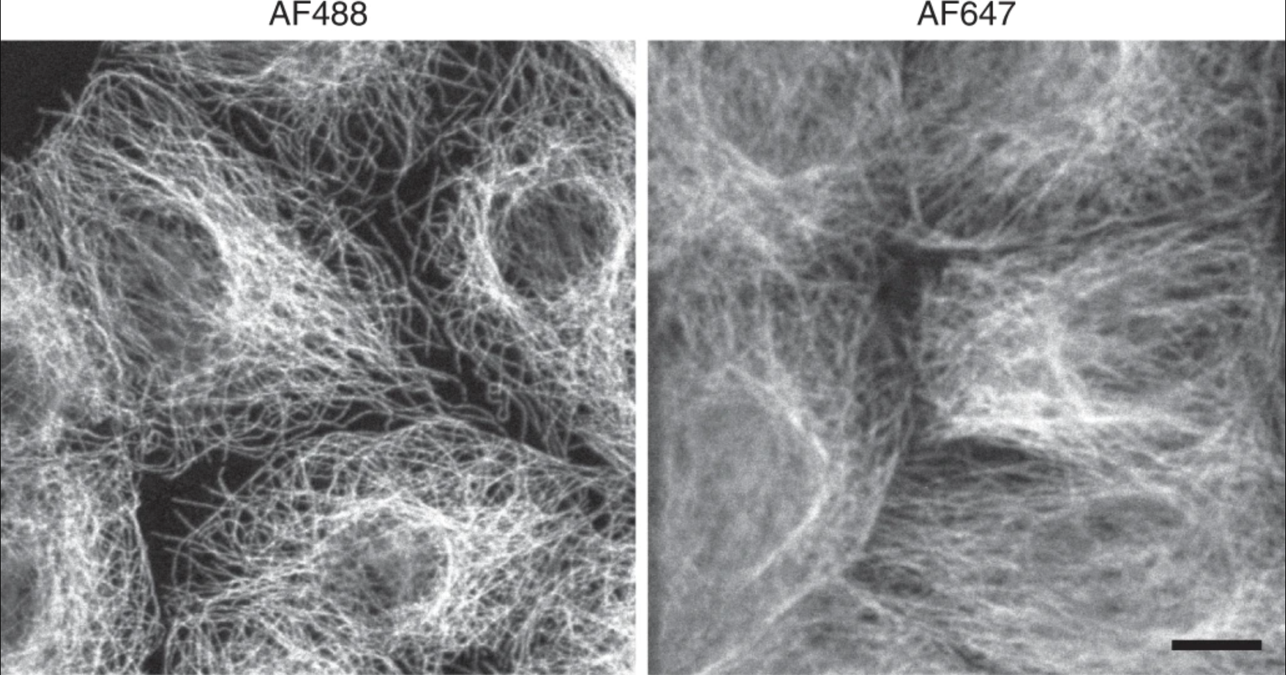
Figura 5 Resolución reducida en longitudes de onda de luz más largas. Los microtúbulos fotografiados con una longitud de onda de luz más corta muestran una resolución más alta que los fotografiados con longitudes de onda más largas. Adaptado de Jonkman J., Brown C.M., Wright G.D et al. Tutorial: orientación para la microscopía confocal cuantitativa. Nat Prot 15, (2020) 5#
Corrección de color: cuando se realiza una microscopía multicolor, es importante elegir una lente objetivo etiquetada como «Apo» o «Super Apo», ya que estas lentes se corrigen para enfocar de 3 a 6 colores en el mismo plano al mismo tiempo. Los lentes
Fluorgeneralmente enfocarán dos colores a la vez.Distancia focal: La distancia de trabajo o distancia focal (WD) da la distancia en milímetros que la lente puede enfocar en la muestra. Esta distancia incluye también el cubreobjetos y los medios de montaje. Si toma imágenes de una muestra gruesa y/o si necesita obtener imágenes lejos de la superficie de la muestra, es importante asegurarse de que la lente tenga una distancia de trabajo suficiente.
Conjuntos de filtros#
It is important to make sure that the microscope that you want to image on has the correct filter sets for the fluorophores you wish to use. See the section on bleedthrough for more information.
Muestreo Z#
If you wish to capture multiple z sections, the spacing of these sections is important if you wish to be able to perform an accurate 3D reconstruction. SVI has a fuller mathematical explanation of this,as well as an easy-to-use online calculator that you can use to calculate the optimal z section spacing for your imaging conditions.
Potencia de adquisición/velocidad#
The amount of signal captured from any fluorophore will be related not just to the intrinsic brightness of the fluorophore, but also the amount of excitation light it is exposed to (due to duration, power, or both) as well as amount of time and signal multiplication that happens at the detector (typically a camera or a photomultiplier tube (PMT)). An optimal experiment is typically one that minimizes the amount of light hitting the sample (to reduce photobleaching and/or phototoxicity) while achieving adequate fluorescent signal and in minimal time on the equipment. How exactly to balance these competing factors will depend on the exact biology being studied and the researcher’s constraints.
